Assistance médicale à la procréation
Cahiers Formation du Moniteur
Ordonnance
Auteur(s) : CAHIER COORDONNÉ PAR NATHALIE BELIN ET ALEXANDRA BLANC PHARMACIENNES, SOUS LA RESPONSABILITÉ DE FLORENCE BONTEMPS , DIRECTRICE SCIENTIFIQUE.
ANALYSE D’ORDONNANCE
LISA ET LUCAS COMMENCENT UN PROTOCOLE DE FIV AVEC ICSI
RÉCEPTION DE L’ORDONNANCE
POUR QUI ?
Lisa N., 30 ans.PAR QUEL MÉDECIN ?
Le gynécologue du centre d'assistance médicale à la procréation (AMP).L’ORDONNANCE EST-ELLE CONFORME À LA LÉGISLATION ?
Oui. La prescription de ménotropine, cétrorelix et choriogonadotropine alfa est réservée à certains spécialistes dont les gynécologues. A la suite du protocole de soins envoyé par le médecin, l’Assurance maladie délivre à la patiente une attestation de prise en charge à 100 % pour les bilans et traitements en AMP valable 2 ans. Les actes d’AMP sont pris en charge jusqu’au 43e anniversaire de la femme à hdiv de 4 FIV maximum.QUEL EST LE CONdiv DE L’ORDONNANCE ?
QUE SAVEZ-VOUS DE LA PATIENTE ?
Lisa a arrêté la prise d’une pilule œstroprogestative il y a 8 mois. Ses règles ont toujours été plus ou moins régulières depuis sa puberté, avec parfois une aménorrhée sur 1 ou 2 cycles mais sans que ceci ait conduit jusqu’à présent à des recherches plus poussées. L’absence de grossesse après plusieurs mois d'arrêt de toute contraception a amené son gynécologue à réaliser une échographie pelvienne qui a mis en évidence un syndrome des ovaires polykystiques. Le médecin l’a alors orientée vers un centre d’AMP qui a mis également en évidence une oligo-asthéno-tératospermie chez son compagnon, Lucas.QUEL ÉTAIT LE MOTIF DE LA CONSULTATION ?
La consultation avait pour objectif la mise en place d’une tentative de FIV avec ICSI.QUE LUI A DIT LE MÉDECIN ?
La prise de Provames, au 22e jour du cycle, va permettre une meilleure planification du cycle de stimulation. Dès l’apparition des saignements, Mme N. devra contacter le centre d’AMP afin de savoir quand commencer les injections de Ménopur qui permettront la maturation de plusieurs follicules ovariens.Le médecin a expliqué qu’un blocage des sécrétions hypophysaires, par Cetrotide, était nécessaire pour un bon contrôle de la stimulation ovarienne. Quand un nombre satisfaisant de follicules aura atteint la taille adéquate, l’ovulation sera déclenchée par Ovitrelle. La ponction ovocytaire et le recueil des spermatozoïdes auront lieu 36 heures après le déclenchement. Le transfert embryonnaire se fera 2 à 6 jours après.
VÉRIFICATION DE L’HISTORIQUE PATIENT
Lisa N. ne prend aucun traitement particulier.LA PRESCRIPTION EST-ELLE COHÉRENTE ?
QUE COMPORTE LA PRESCRIPTION ?
Acide folique : indiqué en prévention des anomalies embryonnaires du tube neural.Traitement estrogénique (Provames) : utilisé ici hors AMM.
Ménotropine : gonadotrophine humaine d’origine urinaire à activité FSH et LH.
Cétrorelix : antagoniste des récepteurs de la GnRH, permettant une inhibition des sécrétions de FSH et de LH.
Choriogonadotropine alfa : analogue de la gonadotrophine chorionique humaine (hCG) permettant le déclenchement de l’ovulation en induisant la maturation folliculaire finale.
Progestérone par voie vaginale : indiquée en supplémentation lutéale dans les protocoles de FIV.
EST-ELLE CONFORME AUX RÉFÉRENTIELS ?
Oui. Le protocole antagoniste est l’un de ceux classiquement utilisés lors de FIV. Il a notamment l’avantage d’induire moins de risque d’hyperstimulation ovarienne et permet de mieux gérer cet effet indésirable, en particulier chez une patiente présentant un syndrome des ovaires polykystiques qui est lui même un facteur de risque d’hyperstimulation ovarienne. Par ailleurs, l’oligoasthénotérato-spermie justifie une FIV avec ICSI : une FIV classique induirait dans ce condiv un risque d’échec trop important.Au cours de ce type de protocole, l’antagoniste, qui réalise un blocage immédiat des sécrétions hypophysaires contrairement à l’agoniste, est généralement débuté après les gonadotrophines vers le 5e ou 6e jour de la stimulation.
Y A-T-IL DES CONTRE-INDICATIONS POUR LA PATIENTE ?
Non. Mme N. ne présente pas d’antécédent de cancer hormonodépendant qui remettrait en cause le protocole d’AMP, ni d'antécédent thrombo-embolique qui justifierait des adaptations de traitement.LES POSOLOGIES SONT-ELLES COHÉRENTES ?
Ménopur : selon le RCP, la posologie initiale recommandée est de 150 à 225 UI. Elle est établie précisément par le médecin à partir de l’évaluation de la réserve ovarienne (reposant sur le dosage de l’AMH et le compte des follicules antraux), de l’âge et du poids de la patiente. Elle est ensuite adaptée à la réponse individuelle au traitement.Cetrotide : la posologie est d’une injection quotidienne de 0,25 mg.
Ovitrelle : la posologie est d’une injection unique de la totalité du stylo à heure précise, après la dernière administration de gonadotrophine.
Les posologies des autres traitements ne posent pas de problème. A noter que la posologie de Provames est plus importante que celle indiquée dans l’AMM.
LA PRESCRIPTION POSE-T-ELLE UN PROBLÈME PARTICULIER ?
Les injections doivent avoir lieu à heure précise selon les indications notées sur l’ordonnance ou données ultérieurement. Il est nécessaire de planifier les rendez-vous avec l’infirmière qui pourra montrer à la patiente comment pratiquer les injections (Ménopur, Cetrotide, Ovitrelle).LE TRAITEMENT NÉCESSITE-T-IL UNE SURVEILLANCE PARTICULIÈRE ?
La surveillance hormonale (dosage de l’estradiol, de la LH et de la progestérone) et échographique est indispensable pour surveiller la croissance folliculaire et éviter une hyperstimulation ovarienne en ajustant les doses de gonadotrophines.QUELS CONSEILS D’ADMINISTRATION DONNER ?
Il s’agit d’une première délivrance. Les traitements injectables nécessitent des explications.UTILISATION
Le matériel nécessaire à la reconstitution et à l’injection des 3 médicaments est fourni, sauf les tampons d’alcool pour Ovitrelle (prévoir le nécessaire, le cas échéant).Ménopur : 1 flacon permet la réalisation de 3 injections à 187,5 UI. La solution est reconstituée à l’aide de la seringue préremplie de solvant injecté dans le flacon de poudre. La seringue graduée permet de prélever la quantité de ménotropine prescrite.
Cetrotide : une fois la solution reconstituée après ajout du solvant dans le flacon de poudre, la totalité de la solution est injectée.
Ovitrelle : chaque seringue préremplie est à usage unique. La mollette doit être tournée jusqu’à « 250 ».
En pratique : se laver les mains avant toute manipulation. Après désinfection du site d’injection, abdomen le plus souvent ou haut de la cuisse, l’aiguille est insérée dans un pli cutané selon un angle de 45 à 90 °. Un léger massage circulaire à l’aide du tampon d’alcool aide ensuite à la dispersion du produit.
CONSERVATION
Ménopur : au réfrigérateur entre 2 et 8 °C. Après reconstitution, la solution peut être conservée pendant 28 jours maximum à une température ne dépassant pas 25 °C.Cetrotide : au réfrigérateur entre 2 et 8 °C ou 3 mois maximum à température ambiante.
Ovitrelle : au réfrigérateur entre 2 et 8 °C.
Pour limiter les douleurs à l’injection, les médicaments conservés au froid doivent être sorties du réfrigérateur 15 à 30 minutes avant l’injection.
QUE FAIRE EN CAS D’OUBLI ?
En cas d’oubli de Ménopur, contacter rapidement le médecin. Cetrotide peut être injecté dès la constatation de l’oubli.QUELS SONT LES PRINCIPAUX EFFETS INDÉSIRABLES ?
Les réactions au point d’injection liées aux différents traitements injectables sont fréquentes (douleur, hématome, irritations).Le cétrorélix peut notamment induire des céphalées et des nausées.
Les gonadotrophines et Ovitrelle peuvent être à l’origine de céphalées et d’un syndrome d’hyperstimulation ovarienne (SHO) d’intensité légère à modérée (douleurs abdominales, nausées...), rarement sévère (risque d’épanchement pleural, oligurie...). Un SHO sévère augmente par ailleurs le risque de thrombose veineuse ou artérielle.
Provames expose aussi à un risque thromboembolique veineux et artériel.
QUELS SONT CEUX GÉRABLES À L’OFFICINE ?
Varier à chaque fois les sites d’injection permet de limiter les réactions cutanées locales.Des douleurs abdominales légères à modérées peuvent être prises en charge par du paracétamol ou du phloroglucinol avant une consultation médicale.
QUELS SIGNES NÉCESSITERAIENT D’APPELER LE MÉDECIN ?
Des douleurs abdominales importantes, des nausées, vomissements et/ou diarrhées gênantes, une augmentation brutale du poids, une oligurie et une dyspnée nécessitent une consultation médicale rapide (suspicion de SHO).Douleurs et œdème d’un membre ou douleurs dans la poitrine font suspecter des manifestations thromboemboliques.
CONSEILS COMPLÉMENTAIRES
Bien respecter le protocole établi. Au moindre doute, appeler le centre d’AMP. Les 10 à 15 jours de stimulation sont contraignants. Prévoir autant que possible une certaine souplesse dans son emploi du temps.
qu’en pensez-vous ?
Vous apportez les médicaments et Lisa en profite pour regarder la notice de Provames qu’elle doit commencer dans 5 jours. Elle s’aperçoit que Provames est indiqué chez des femmes ménopausées et ne comprend pas du coup l’intérêt de ce traitement ? Que lui répondez-vous ?
1) Ce traitement augmente les chances de succès de la tentative de FIV
2) Il permet une meilleure planification du cycle de stimulation
Réponse : Un prétraitement (selon le cas estrogénique, estroprogestatif ou progestatif) est parfois proposé avant un cycle de FIV dans le but surtout de planifier la stimulation. Ce prétraitement vise aussi en théorie à empêcher le petit pic de sécrétion de FSH qui précède les règles et qui lance le recrutement folliculaire du cycle à venir. Le prétraitement, en bloquant cet effet, permettrait ainsi une meilleure « synchronisation » de la cohorte folliculaire pour recruter davantage de follicules de la même taille, en même temps. Les études concernant ce point ne sont cependant pas probantes. La 2e réponse est donc la bonne.
qu’en pensez-vous ?
Lisa se rend dans quelques jours à un concert et vous demande si ce jour-là, l’injection pourra être réalisée dans l’après-midi plutôt que le soir.
1) oui sans problème
2) non
Réponse : Les injections de gonadotrophines se font le soir, ce qui permet l’adaptation éventuelle de la dose en fonction des résultats du monitorage (dosages hormonaux, échographie selon le cas) dans la journée. L’antagoniste est administré en même temps en un site d’administration distinct. Ménopur une fois reconstitué et Cetrotide se conservent à température ambiante et tout le matériel d’injection est fourni. Les injections peuvent donc être facilement transportées et réalisées sur place. La réponse 2 est la bonne.
PATHOLOGIE
L’INFERTILITÉ EN 4 QUESTIONS
1 QUELLES SONT LES CAUSES?
CHEZ LA FEMME
Anovulations ou dysovulations : soupçonnées devant une aménorrhée ou des irrégularités menstruelles, mais des cycles réguliers n’éliminent pas un trouble de l’ovulation.Origine :syndrome des ovaires polykystiques, insuffisance ovarienne (d’origine génétique, ou post-chimio ou radiothérapie...), cause endocrinienne (hyperprolactinémie, dysthyroïdie et notamment hypothyroïdie, hyperandrogénie).
Anomalies tubaires : cause majeure d’infertilité. L’obstacle tubaire peut être dû à des séquelles d’infection génitale, notamment une salpingite, un traumatisme chirurgical ou une endométriose.
Autres : notamment anomalies du col utérin ou de la glaire cervicale liées à des interventions chirurgicales (conisation, curetage...), exposition in utero au diéthylstilbestrol (peut concerner les femmes nées avant 1977) à l’origine de perturbations de la fonction ovarienne et/ou de malformations utérines.
CHEZ L’HOMME
Oligo-asthéno-tératospermie (OAT): il s’agit d’anomalies du sperme détectées lors de la réalisation d’un spermogramme avec spermocytogramme, portant notamment sur les caractéristiques des spermatozoïdes : concentration (oligospermie), mobilité (asthénospermie), morphologie (tératospermie). Les causes sont multiples : troubles hormonaux, infections ou séquelles d’infections, présence d’anticorps antispermatozoïdes...Autres : malformations des voies génitales, éjaculations rétrogrades (vers la vessie), anomalies génétiques, varicocèle, effets de chimio ou radiothérapie...
2 QUELS FACTEURS INFLUENCENT LA FERTILITÉ ?
Chez la femme, les chances de grossesse diminuent de façon importante après 35 ans et le risque de fausses couches augmente. Chez l’homme, l’âge est associé à une baisse de la fertilité mais à un degré moindre et à un âge plus avancé.Chez la femme, l’obésité ou la maigreur ou une activité sportive intense peuvent entraîner des troubles de l’ovulation. Chez l’homme, une exposition professionnelle à la chaleur, aux radiations ou à des toxiques (pesticides...) peut être en cause.
Chez l’homme et la femme, le tabac, l’alcool et la consommation de drogues (cannabis, héroïne...) affectent la fertilité.
3 COMMENT EXPLORER UNE INFERTILITÉ ?
L’interrogatoire précise la sexualité du couple (fréquence et moment des rapports, difficultés éventuelles...), le mode de vie (activité professionnelle, exposition à des toxiques...), l’âge, le poids, la taille, les antécédents médicaux (infections génitales, oreillons chez l’homme...) ou de grossesse, ou de paternité avec une autre femme pour l’homme, des signes évocateurs de troubles endocriniens (hirsutisme, gynécomastie chez l’homme...).Chez la femme sont demandés les caractéristiques du cycle, la courbe de température, un bilan hormonal et un bilan infectiologique préconceptionnel. L’échographie pelvienne étudie l’utérus et ses annexes et évalue la réserve ovarienne (nombre de follicules antraux). Selon le cas, sont réalisées une hystérosalpingographie (explore la perméabilité tubaire), une biopsie d’endomètre, une cœlioscopie (notamment en cas de suspicion d’endométriose).
Chez l’homme, en plus du spermogramme, la spermoculture et le prélèvement d’urines recherchent une infection (chlamydiae…). Selon le cas, sont réalisés des dosages hormonaux, une échographie pelvienne, un bilan immunologique (recherche d’anticorps antispermatozoïdes).
Pour le couple, le test post-coïtal de Hühner analyse au microscope le comportement des spermatozoïdes dans la glaire cervicale en période pré-ovulatoire et la qualité de celle-ci. Les sérologies VIH, hépatites B et C et syphilis sont obligatoires avant le recours aux techniques d’AMP. Selon le cas, sont réalisés un caryotype et un bilan génétique complémentaire (si azoospermie ou oligospermie sévère, avortements spontanés à répétition).
4 QUELLES SONT LES TECHNIQUES D’AMP ?
Les techniques par manipulation des gamètes permettent de remédier à l’infertilité du couple. Elles permettent aussi d’éviter la transmission d’une maladie grave à l’enfant ou à l’un des membres du couple, en ayant notamment recours à un don de gamète ou à la réalisation d’un diagnostic préimplantatoire pour ne transférer que des embryons non atteints par une pathologie génétique ou chromosomique grave.Insémination intra-utérine(ou artificielle) : elle consiste à déposer au niveau de la cavité utérine une préparation de spermatozoïdes pour favoriser la rencontre des gamètes mâles et femelles. Elle s’accompagne généralement d’une stimulation ovarienne. Principales indications : altérations modérées du sperme, stérilités inexpliquées ou dysovulations après échec d’une induction simple d’ovulation, troubles de l’éjaculation, inséminations avec sperme de donneur ou autoconservé. Taux moyen de naissances : environ 10 %, s’élevant à 18 % en cas de don de sperme.
Fécondation in vitro (FIV): la rencontre des gamètes, la fécondation et les premiers stades de développement de l’embryon sont réalisés in vitro avant transfert des embryons dans la cavité utérine. Principales indications : stérilités ou altération tubaires, insuffisances spermatiques modérées, stérilités inexpliquées ou anovulation après échec notamment d’inséminations artificielles... Taux moyen de naissances : environ 19 %.
Fécondation in vitro avec micromanipulation (ou ICSI, Intra cytoplasmic sperm injection) : identique à la FIV mais un seul spermatozoïde, sélectionné, est injecté dans le cytoplasme de l’ovocyte. Principales indications : insuffisances spermatiques sévères, échec de FIV, diagnostic préimplantatoire… Taux moyen de naissance : environ 20 %.
Congélation des gamètes et d’embryons : elle peut être réalisée pour préserver la fertilité d’un individu avant certains traitements gonadotoxiques ou gamétotoxiques ou être nécessaire juste avant une FIV (si le prélèvement du sperme ne peut avoir lieu le même jour que la ponction ovocytaire, par ex.). Les embryons surnuméraires conçus lors d’une FIV et non transférés peuvent également être cryoconservés pour un transfert ultérieur. S’il n’y a plus de projet parental, ils pourront faire l’objet d’un don (après accord des 2 membres du couple) pour un autre couple infertile. Enfin, en cas d’absence de gamète chez un seul membre du couple, il peut être fait appel à un don de sperme ou d’ovocytes.
Syndrome des ovaires poly-kystiques
Hyperandrogénie associée à un trouble de la folliculogénèse.
Endo-métriose
Présence de tissu endométrial en dehors de la cavité utérine (trompes, ovaire...). L’infertilité, non systématique, peut être due à l’inflammation locale, à des kystes ovariens ou à des adhérences.
Conisation
Technique chirurgicale consistant en l’ablation d’une partie du col de l’utérus.
Spermo-gramme
Examen biologique des différents paramètres constituants le sperme.
Spermo-cytogramme
Analyse cytologique et morphologique des spermatozoïdes au microscope après fixation et coloration.
Varicocèle
Dilatation des veines du cordon spermatique.
Courbe de température
Réalisée sur 2 ou 3 cycles. Prise de la température corporelle au réveil avant le lever, toujours avec le même thermomètre et par la même voie. Le décalage thermique (augmentation de 0,5 à 0,6 °C de la température due à la sécrétion de progestérone) confirme la transformation du follicule dominant en corps jaune. L’ovulation a en général lieu la veille du décalage thermique.
en chiffres
Les chances de grossesse, en l’absence de toute anomalie féminine ou masculine, sont d’environ 25 % par cycle à 25 ans, 12 % à 35 ans, 6 % à 40 ans.
En France, environ 16 % des couples consultent pour un désir d’enfant.
En 2015, 3,1 % des enfants nés en France sont issus d’une AMP (24 839 enfants) dont 24,8 % (6 160 enfants) ont été conçus par insémination intra-utérine.
Physiopathologie du cycle ovarien
L'hypothalamus sécrète de façon pulsatile la GnRH (gonadotropin releasing hormone) qui régule la sécrétion hypophysaire de FSH (follicle stimulating hormone) et de LH (luteinizing hormone), modulant à leur tour la croissance des follicules ovariens. L'hypothalamus, l'hypophyse et l'ovaire (axe gonadotrope) sont liés par un système de rétrocontrôle, négatif ou positif.
Phase folliculaire : la FSH assure avec la LH le développement des follicules ovariens dont un seul par cycle parvient à maturité. Le follicule sécrète de l’estradiol stimulant sa propre croissance et induisant, lorsqu’il est à maturité, le pic de LH qui va se déclencher environ 36 heures après l'ovulation.
Phase lutéale : le follicule se transforme en corps jaune qui secrète surtout de la progestérone. En l'absence de grossesse, le corps jaune involue. La chute des taux hormonaux entraîne conjointement l’apparition des règles et le recrutement de follicules primaires en vue du prochain cycle.
THÉRAPEUTIQUE
COMMENT SE DÉROULE UNE PRISE EN CHARGE EN AMP ?
STRATÉGIE THÉRAPEUTIQUE
A ce jour en France, l’AMP exclut les femmes seules et les couples homosexuels. Les tentatives sont prises en charge à 100 % par l’Assurance maladie jusqu’au 43e anniversaire de la femme à raison de 6 tentatives d’insémination intra-utérine et 4 tentatives de FIV, avec ou sans micromanipulation. Les inductions simples d’ovulation avec rapports sexuels programmés font partie des traitements médicaux de l’infertilité mais ne rentrent pas dans le cadre de l’AMP.Quelle que soit la technique d’AMP envisagée, le protocole suit le même déroulement : une phase initiale de stimulation ovarienne permettant le développement d’un ou plusieurs follicules ovariens ; le déclenchement de l’ovulation ; le soutien de la phase lutéale afin de favoriser les chances d’implantation de l’embryon.
Pour contrôler la phase de stimulation et éviter un pic prématuré endogène de LH et une ovulation spontanée, on a recours aux analogues de la GnRH, agonistes ou antagonistes, qui bloquent les sécrétions hypophysaires de LH et FSH.
STIMULATION OVARIENNE
Selon le cas, elle doit permettre l’obtention d’un à deux follicules ovariens (« recrutement mono- ou paucifolliculaire »), ou d’une dizaine de follicules ovariens (recrutement « plurifolliculaire »).RECRUTEMENT MONO- OU PAUCIFOLLICULAIRE
Il est indiqué lors de rapports sexuels programmés ou lors d’une insémination intra-utérine (IIU). La stimulation ovarienne débute vers le 6e jour du cycle.Lors de rapports sexuels programmés, le citrate de clomifène peut être indiqué notamment en cas de syndrome des ovaires polykystiques. En cas d’échec, des gonadotrophines à faibles doses sont utilisées.
Lors d’IIU, on a recours aux gonadotrophines, toujours à faibles doses (environ 75 à 150 UI/jour pendant 5 à 10 jours en général). Celles-ci peuvent être associées à un antagoniste de la GnRH pour un meilleur contrôle du moment de l’ovulation.
RECRUTEMENT PLURIFOLLICULAIRE
L’obtention de plusieurs follicules s’impose lors d’une FIV afin d’augmenter les chances d’obtenir in vitro un embryon de qualité. Un ou 2 embryons seront transférés dans la cavité utérine. Les embryons surnuméraires, de qualité et non transférés, seront cryoconservés en prévision d’un transfert ultérieur.Les gonadotrophines, prescrites à dose élevée (150 à 300 UI/jour), sont systématiquement associées à un analogue de la GnRH dont le choix, antagoniste ou agoniste, est décidé en fonction du condiv de l’infertilité ou de la stérilité du couple, des traitements et résultats antérieurs, de la patiente elle-même (âge, poids, durée des cycles...).
Protocole antagoniste : les gonadotrophines sont débutées en début de cycle. L’antagoniste est introduit généralement après 5 à 6 jours de stimulation. Ce protocole peut être réalisé avec la corifollitropine alfa (Elonva), gonadotrophine ayant une AMM en association à un antagoniste et dont une seule injection sous-cutanée remplace les 7 premières injections quotidiennes d’une gonadotrophine classique. Un protocole antagoniste est parfois associé à un prétraitement estrogénique, estroprogestatif ou progestatif (hors AMM) sur le ou les cycles précédant la stimulation ovarienne dans le but de sa meilleure planification.
Le nombre de protocoles antagonistes est en progression car ils sont mieux tolérés avec un moindre risque d’hyperstimulation ovarienne (voir Complications).
Protocole agoniste : il se décline en version longue ou courte et peut également être associé à un prétraitement (moins fréquemment toutefois lors d’un protocole long).
Protocole agoniste court : l’administration quotidienne d’agoniste par voie nasale (Synarel) ou injectable (Décapeptyl 0,1 mg) se fait en début de cycle. Les gonadotrophines sont débutées quelques jours après. Ce protocole est moins utilisé que le protocole long, car le nombre d’ovocytes recueillis est globalement moindre.
Protocole agoniste long : il commence en milieu de phase lutéale du cycle précédent ou en début de phase folliculaire. Au lieu d’injections quotidiennes d’agoniste, il est possible de recourir à une injection unique d’agoniste retard (Décapeptyl 3 mg, voire Enantone LP 3,75 hors AMM). Une fois la désensibilisation hypophysaire constatée (monitorage), les injections de gonadotrophines peuvent commencer.
MONITORAGE
Il est débuté environ 6 jours après le début de la stimulation : des échographies visualisant les ovaires et l’endomètre ainsi que des dosages hormonaux (estradiol, LH, progestérone) permettent de suivre la croissance folliculaire, d’adapter les posologies et de repérer le meilleur jour pour déclencher l’ovulation (épaisseur de l’endomètre, taille des follicules, taux d’estradiol…).DÉCLENCHEMENT DE L’OVULATION
Il est réalisé par l’administration d’une dose unique de l’analogue de l’hCG (Ovitrelle). L’insémination artificielle, ou dans le cas d’une FIV, la ponction ovocytaire a lieu environ 36 heures après le déclenchement. Les ovocytes recueillis sont mis en présence des spermatozoïdes au laboratoire. Le transfert du ou des embryons sélectionnés a lieu 2 à 3 jours ou parfois 5 à 6 jours après le déclenchement.SOUTIEN DE LA PHASE LUTÉALE
Visant à faciliter l’implantation de l’embryon, il consiste en un traitement par progestérone débuté après le déclenchement et poursuivi les premières semaines de grossesse. Dans certains cas (insuffisance gonadotrope), le soutien de la phase lutéale est réalisé par injection d’hCG (Ovitrelle hors AMM). Un dosage sanguin de bêtahCG est réalisé 14 jours après l’insémination ou la ponction ovarienne. En cas de test positif, un nouveau contrôle est réalisé pour confirmer la bonne évolution de la grossesse.COMPLICATIONS
Outre les effets indésirables imputés directement aux médicaments de l’AMP, la stimulation ovarienne peut entraîner des complications, plus fréquentes lors de FIV : risque accru de grossesses multiples, de complications thromboemboliques, et risque de syndrome d’hyperstimulation ovarienne (SHO). Ce dernier est plus fréquent avec des protocoles incluant des agonistes. Il se traduit par une augmentation anormale du volume de l’ovaire et une vasodilatation artérielle avec possible hypovolémie.Un SHO sévère est un facteur de risque de thrombose veineuse ou artérielle.
TRAITEMENTS
ANALOGUES DE LA GNRH
Ils favorisent un recrutement folliculaire optimal en bloquant les sécrétions hypophysaires afin de ne pas interférer avec les secrétions de gonadotrophines endogènes.AGONISTES DE LA GNRH
Ils agissent en 2 étapes. Dans un premier temps, leur administration provoque une libération massive de gonadotrophines, FSH et LH : c’est l’effet « flare up ». Puis, après quelques jours, les taux de gonadotrophines s’effondrent, réalisant un blocage de l’axe hypophyso-gonadique. Un agoniste retard (forme à libération prolongée) induit une désensibilisation hypophysaire plus profonde et plus durable permettant une unique administration dans les protocoles longs. Différentes voies d’administration sont disponibles : injectable ou nasale.Effets indésirables les plus fréquents : bouffées de chaleur, troubles de la libido, prise de poids, réactions et douleurs au point d’injections, sécheresse vaginale, myalgies et douleurs au point d'injection. Pour la voie nasale : rhinite.
ANTAGONISTES DE LA GNRH
Contrairement aux agonistes, le blocage hypophysaire est immédiat.Effets indésirables : globalement mieux tolérés que les agonistes, ils peuvent néanmoins induire des céphalées, des nausées et des réactions au site d’injection. La durée du traitement étant moins longue que sous agonistes, ils n’entraînent généralement pas de symptômes ménopausiques.
INDUCTEURS DE L’OVULATION
GONADOTROPHINES
Agissant sur l’ovaire en permettant le développement de follicules matures, elles sont utilisées dans toutes les techniques d’AMP mais aussi hors AMP, par exemple lors d’inductions simples de l’ovulation avec rapports programmés.Elles se distinguent par leur activité FSH, LH ou mixte. Certaines gonadotrophines sont obtenues par extraction urinaire (urofollitropine et ménotropine), les autres sont recombinantes, obtenues par génie génétique.
ANALOGUE DE L’HCG
Seule la spécialité Ovitrelle est disponible. Elle s'administre en une dose unique à heure précise. Elle est parfois utilisée hors AMM pour le soutien de la phase lutéale.EFFETS INDÉSIRABLES COMMUNS
Très fréquents : céphalées, kystes ovariens, réactions au site d’injection (douleur, érythème, hématome, œdèmes). Fréquents : douleurs et distension abdominales, nausées, vomissements, diarrhées en rapport avec un syndrome d’hyperstimulation ovarienne (SHO) d’intensité légère à modéré. Des vertiges, une fatigue ou une sensation de malaise sont également rapportés.Rarement : SHO sévère suspecté devant œdème, essoufflement, oligurie et accident thrombo-embolique associé ou non à un SHO.
STATUTS
La prescription des gonadotrophines et des antagonistes de la GnRH est notamment réservée aux spécialistes en endocrinologie, en gynécologie et obstétrique. Le renouvellement est réservé à ces mêmes spécialistes.MÉDICAMENTS NON SPÉCIFIQUES À L’AMP
CITRATE DE CLOMIFÈNE
Il a l’AMM dans le cadre des protocoles d’AMP mais n’est plus utilisé dans ce condiv. Il reste indiqué dans certaines infertilités comme le syndrome des ovaires polykystiques lors de rapports sexuels programmés. La dose initiale est d’un comprimé à 50 mg par jour pendant 5 jours, à débuter au 2e ou 3e jour du cycle et à ajuster en fonction du monitorage.Effets indésirables : insuffisance de glaire cervicale, apparition ou aggravation d’une endométriose, bouffées vaso-motrices, hyperstimulation ovarienne, kystes fonctionnels, troubles de la vision imposant l’arrêt définitif du traitement, céphalées, troubles gastro-intestinaux, risque de grossesses multiples.
POMPE À GNRH
La gonadoréline (Lutrelef), un analogue de la GnRH, est utilisée à l’aide d’un système de pompe (Lutrepulse) permettant son injection de façon pulsatile par voie sous-cutanée. Elle induit ainsi une libération physiologique de FSH et LH. Ses indications sont les anovulations ayant pour cause un hypogonadisme hypogonadotrope, avec une hypophyse intacte dans le cadre de rapports sexuels programmés. Cette stimulation est associée à un monitorage pour limiter le risque de grossesses multiples.PROGESTÉRONE
Elle est utilisée en soutien de la phase lutéale par voie vaginale, à la posologie de 400 à 600 mg par jour en 2 à 3 prises.Elle est disponible depuis peu dans cette indication par voie injectable (Progiron, 25 mg en IM ou SC).
PERSPECTIVES
En 2018, la révision de la loi de bioéthique pourrait permettre une ouverture de l’AMP à toutes les femmes. Hypo-gonadisme hypo-gonadotrope
Caractérisé par une diminution des taux d’estradiol associée à des valeurs de FSH et LH normales à basses.
SHO sévère
Le syndrome d'hyperstimulation ovarienne peut s'accompagner de complications à type d'ascite, d'épanchement pleural, de dyspnée, d'oligurie, d'événements thrombo-emboliques et de torsion ovarienne.
CE QUI A CHANGÉ
Apparus
- Fyrémadel Gé fin 2017 : générique de l’orgalutran (Ganirélix),.
- Bemfola, Ovaleap en 2016 : biosimilaires* de la follitropine alfa (Gonal-F).
- FertistartKit en 2016 : association de ménotropine et d’hCG.
- Crinone en 2015 : supplémentation en progestérone en gel vaginal, indiqué pendant la phase lutéale dans le cadre d’une AMP.
- Progiron 25 mg en 2015 : solution injectable IM ou SC de progestérone indiquée dans le cadre d’une AMP chez les patientes présentant une intolérance aux préparations vaginales ou ne pouvant les utiliser.
- Elonva (corifollitropine alfa) en 2014 : gonadotrophine à durée d’activité FSH prolongée.
Disparu
Gonadotrophine Chorionique Endo : arrêt de commercialisation en août 2016.
* Interchangeabilité envisageable uniquement par le prescripteur après accord du patient.
vigilance !
Les principales contre-indications des traitements sont les suivantes :
Gonadotrophines : kyste ovarien autre qu’un syndrome des ovaires polykystiques, saignements gynécologiques d'étiologie inconnue, tumeurs de l'ovaire, du sein, de l'utérus, de l'hypophyse ou de l'hypothalamus.
Antagoniste de la GnRH : insuffisance rénale modérée ou sévère.
Citrate de clomifène : troubles visuels pendant le traitement ou lors de traitements antérieurs, saignements gynécologiques d'étiologie inconnue, kyste ovarien, tumeurs hormonodépendantes.
Pointdevue
Dr Nathalie Massin, endocrinologue, Centre d’assistance médicale à la procréation, Centre Hospitalier Intercommunal de Créteil (Val-de-Marne)
« Le taux de naissance est le même sous protocole agoniste ou antagoniste »
Les protocoles antagonistes et agonistes donnent-ils les mêmes résultats ?
Oui. Les études les plus récentes montrent qu’on obtient en moyenne un ovocyte de moins par tentative de FIV avec un protocole antagoniste par rapport à un protocole agoniste long, mais au final, le nombre de naissances est équivalent pour ces deux protocoles. Le protocole antagoniste étant mieux toléré, avec surtout un moindre risque de syndrome d’hyperstimulation ovarienne (SHO), il est souvent préféré et s’impose systématiquement chez des patientes présentant un facteur de risque de SHO : âge jeune, syndrome des ovaires polykystiques, antécédent de SHO lors d’un précédent traitement. Ces situations nécessitent aussi une adaptation des doses des gonadotrophines. De plus, lors d’un traitement antagoniste, l’injection d’Ovitrelle sera suspendue si le risque de SHO est important, mais on peut quand même, dans certains cas, déclencher l’ovulation par un agoniste, en utilisant son effet « flare up » (hors AMM).
La prise d’aspirine à faible dose présente-t-elle un intérêt ?
Aucun, hormis dans certaines indications très spécifiques, comme un risque thrombotique.
LAURA, 32 ANS, SANS EMPLOI
L’AMP VUE PAR LES PATIENTS
IMPACT PSYCHOLOGIQUE
L’annonce d’une infertilité, féminine ou masculine, représente un moment difficile qui bouleverse la vie du couple. Le conjoint infertile endosse la responsabilité et a souvent tendance à se dévaloriser : sentiment de remise en cause de la virilité chez l’homme, diminution de l’estime de soi liée à l’incapacité d’être mère chez la femme.Les protocoles d’AMP sont éprouvants physiquement et moralement : les périodes d’espoir alternent souvent avec des périodes de déception.
IMPACT SUR LA VIE QUOTIDIENNE
Souvent, les couples ne souhaitent pas partager leurs difficultés à avoir des enfants. Les contraintes des traitements (prises de sang tôt le matin, échographies dans la journée, injections à heure fixe le soir) obligent à beaucoup de disponibilité, imposant parfois des retards au travail ou la nécessité de poser des congés ou de refuser des invitations.Les contraintes médicales associées au stress et à l’angoisse perturbent l’intimité du couple et la spontanéité des rapports sexuels.
À DIRE AUX PATIENTES
A PROPOS DE L’AMP
Le parcours des patientes en AMP dure parfois plusieurs années échelonnées par plusieurs tentatives d’insémination intra-utérine et/ou de FIV.Les parcours sont difficiles et stressants. Quelques publications sur ce sujet ont montré que prendre du recul et gérer le stress augmentent les chances de grossesse en AMP. Il faut donc essayer de conserver un état d’esprit positif, se détendre en pratiquant des activités que l’on aime, essayer d’avoir d’autres objectifs à court et moyen terme pour ne pas penser à avoir un enfant à tout prix et tout de suite.
Un soutien psychologique, proposé dans certains centres d’AMP, peut être important, d’autant plus que l’infertilité génère un sentiment de dévalorisation chez l’un des deux conjoints. Les associations de patients peuvent aussi être utiles.
Selon le cas, on peut rappeler qu’une bonne hygiène de vie concourt à augmenter les chances de fertilité. L’effet délétère du tabagisme sur la fertilité féminine est bien démontré. La maigreur (comportement alimentaire, pratique intensive d’un sport) et plus souvent le surpoids et afortiori l’obésité altèrent les résultats de la prise en charge de l’infertilité quelle qu’elle soit. Chez l’homme, l’impact négatif du tabac, du café, de l’alcool, du stress, de polluants environnementaux est bien démontré.
Au cours d’une FIV, la ponction ovocytaire, sous anesthésie générale, locale ou sous hypnose, peut être suivie de petits saignements qui ne doivent pas inquiéter.
La période d’attente des résultats qui suit l’insémination du sperme ou le transfert d’embryons est particulièrement angoissante. Prévoir durant cette période des activités divertissantes et se faire plaisir (sorties...).
A PROPOS DU TRAITEMENT
Les protocoles sont individualisés et adaptés à chaque couple et n’impliquent donc pas le même suivi et les mêmes contraintes. Il faut s’assurer que le déroulé et les prises des différents traitements sont bien compris en redétaillant chaque étape. Au moindre doute, la patiente ne doit pas hésiter à prendre contact avec le service d'AMP pour adapter le traitement ou poser des questions.Les injections en pratique. Vérifier qui pratique l’injection. Prévoir de donner le contact de quelques infirmiers libéraux. Pour s’affranchir du stress du passage quotidien d’un infirmier, il peut être plus confortable d’être autonome quant aux injections : la patiente elle-même ou son conjoint peut apprendre à les effectuer. Proposer un container adapté pour la récupération du matériel. Vérifier systématiquement la nécessité de joindre le matériel nécessaire aux injections (seringues, aiguilles, alcool). Selon le mode de conservation des produits, prévoir des pochettes isothermes. Même si les modalités de l’injection sont expliquées par l’infirmière, les rappeler : sortir les produits du réfrigérateur 15 à 30 minutes à l’avance, se laver les mains et poser le matériel sur un plan de travail propre, désinfecter la zone d’injection (bas de l’abdomen généralement ou haut de la cuisse) avec de l’alcool, piquer, selon un angle de 45 à 90°, appliquer une compresse ou un tampon d’alcool en massant doucement la zone d’injection.
Gonadotrophines et analogues de la GnRH peuvent être injectés en même temps en 2 sites différents. Les injections se font en soirée à peu près à la même heure chaque jour. Ainsi, selon le monitorage effectué en journée (bilan sanguin, échographie), les doses seront adaptées pour la prochaine injection du soir.
Le déclenchement de l’ovulation par Ovitrelle : l’injection doit être effectuée à un horaire précis dans le cas d’une FIV car elle conditionne l’heure de la ponction ovocytaire réalisée environ 36 heures plus tard. Cet horaire est moins strict dans le cadre d’une insémination intra-utérine.
Les effets indésirables : céphalées, irritabilité, distension abdominale, tension mammaire, troubles digestifs, douleurs au point d’injection sont relativement fréquents. Sueurs, bouffées de chaleur sont possibles sous agonistes de la GnRH.
question de patient Sous Bemfola depuis 8 jours, je commence à avoir des douleurs et des tensions abdominales. Est-ce normal ?
«Oui, le traitement peut occasionner des douleurs pelviennes modérées et parfois des nausées. Des douleurs importantes, notamment avec prise de poids brutale, sensation de malaise, nausées et/ou diarrhées doivent faire suspecter une stimulation ovarienne excessive. Il faut en informer rapidement l’équipe médicale. Le risque de thrombose veineuse est majoré. Selon le cas, le traitement peut être arrêté. La survenue d’une grossesse aggrave le syndrome d’hyperstimulation, la patiente devra donc utiliser des préservatifs ou ne pas avoir de rapports sexuels. »
question de patient Ma compagne peut-elle prendre des compléments alimentaires pour augmenter les chances de réussite ?
«Quelques compléments alimentaires formulés principalement avec du zinc, des vitamines C, E et du groupe B, sont proposés pour améliorer la fertilité. Ils n’ont aucun intérêt démontré lors de protocoles d’AMP. La seule vitamine indispensable est l’acide folique, qui diminue le risque de malformation du tube neural en début de grossesse.»
EN SAVOIR PLUS
FIVFRANCE
fivfrance.org
De nombreuses informations réparties sur deux portails distincts, l’un à destination du grand public, l’autre des professionnels de santé.
Agence de la biomédecine
agence-biomedecine.fr
Les chiffres sur l’AMP, la loi de bioéthique. Le portail destiné au grand public renvoie pour l'AMP au site procreation-medicale.fr.
Association de patients
amphore.fr
Des professionnels de santé (psychologue, sage-femme...) proposent bénévolement leur soutien par le biais de rendez-vous téléphoniques notamment, ou de groupes de parole.
DÉLIVRERIEZ-VOUS CES ORDONNANCES ?
MÉMO DÉLIVRANCE
Gonadotrophines et antagonistes de la GnRH (Cetrotide, Orgalutran, Fyremadel) : prescription notamment réservée aux spécialistes en endocrinologie, en gynécologie et obstétrique.
Agonistes de la GnRH (Synarel, Décapeptyl...) : prescription possible par tout médecin.
La patiente a-t-elle bien compris le déroulé du protocole ?
Quelle que soit la technique choisie, FIV ou IIU, le traitement comporte :
– une phase de stimulation ovarienne induite par des injections quotidiennes de gonadotrophines ;
– l’inhibition des sécrétions endogènes de FSH et LH, susceptibles de perturber la stimulation (avec notamment induction d’une ovulation prématurée), grâce à l’action d’un antagoniste ou d’un agoniste de la GnRH ;
– le déclenchement de l’ovulation (Ovitrelle).
Une surveillance régulière, biologique (taux d’estradiol, LH et progestérone) et échographique, est indispensable.
Sait-elle quand et selon le cas comment réaliser les injections ?
Gonadotrophines et analogues de la GnRH s’injectent en sous-cutanée (sauf Décapeptyl LP 3 mg, en IM) le soir, pour adapter rapidement les doses en fonction des résultats du monitorage. L’injection sous-cutanée d’Ovitrelle s’effectue à heure précise dans le cas d’une FIV car elle conditionne le moment de la ponction ovocytaire.
Vérifier systématiquement les modalités de conservation des produits (à température ambiante sur une durée définie pour certains), et la nécessité de fournir le matériel nécessaire aux injections.
En pratique : sortir selon le cas les produits du réfrigérateur 15 à 30 minutes à l’avance, désinfecter la zone d’injection (bas de l’abdomen généralement ou haut de la cuisse), piquer selon un angle de 45 à 90°, appliquer un tampon d’alcool en massant doucement. Changer à chaque fois les sites d'injection.
Connait-elle les effets indésirables ?
Céphalées, tension abdominale et mammaire, troubles digestifs, douleurs au point d’injection sont fréquents ; des bouffées de chaleur sont possibles sous agonistes.
Des douleurs abdominales importantes et/ou associées à des nausées, diarrhées ou vomissements doivent amener à contacter rapidement le centre d’AMP (suspicion d’hyperstimulation ovarienne). L'apparition d’œdèmes des extrémités ou d'un essoufflement constituent une urgence (suspicion d'un syndrome d'hyperstimulation ovarienne sévère).
NON. Le dosage de 0,1 mg de la triptoréline n’est pas adapté à une injection unique comme semble l’indiquer le libellé de la posologie, mais à des administrations quotidiennes. C’est la référence Décapeptyl LP 3 mg qui permet un blocage prolongé de l’axe hypothalamo-hypophysaire et s’administre à raison d’une injection IM par cycle de stimulation. Il est donc nécessaire de contacter le centre d’AMP.
oui, en donnant des explications. Pergoveris, solution injectable à usage unique, renferme 150 UI de FSH et 50 UI de LH. La posologie s’exprime en unité de FSH. Pour obtenir 300 UI, il faut donc utiliser 2 flacons. Si la patiente réalise elle-même l’injection, l'infirmière pourra lui proposer la technique de reconstitution suivante : injecter un flacon de solvant dans un flacon de poudre, puis prélever et injecter la solution obtenue dans le 2 e flacon, ceci permettant de réduire le volume à injecter. Fournir une seringue de 1 ml, une aiguille pour la reconstitution (type G18) et une pour l'injection SC (type G26).
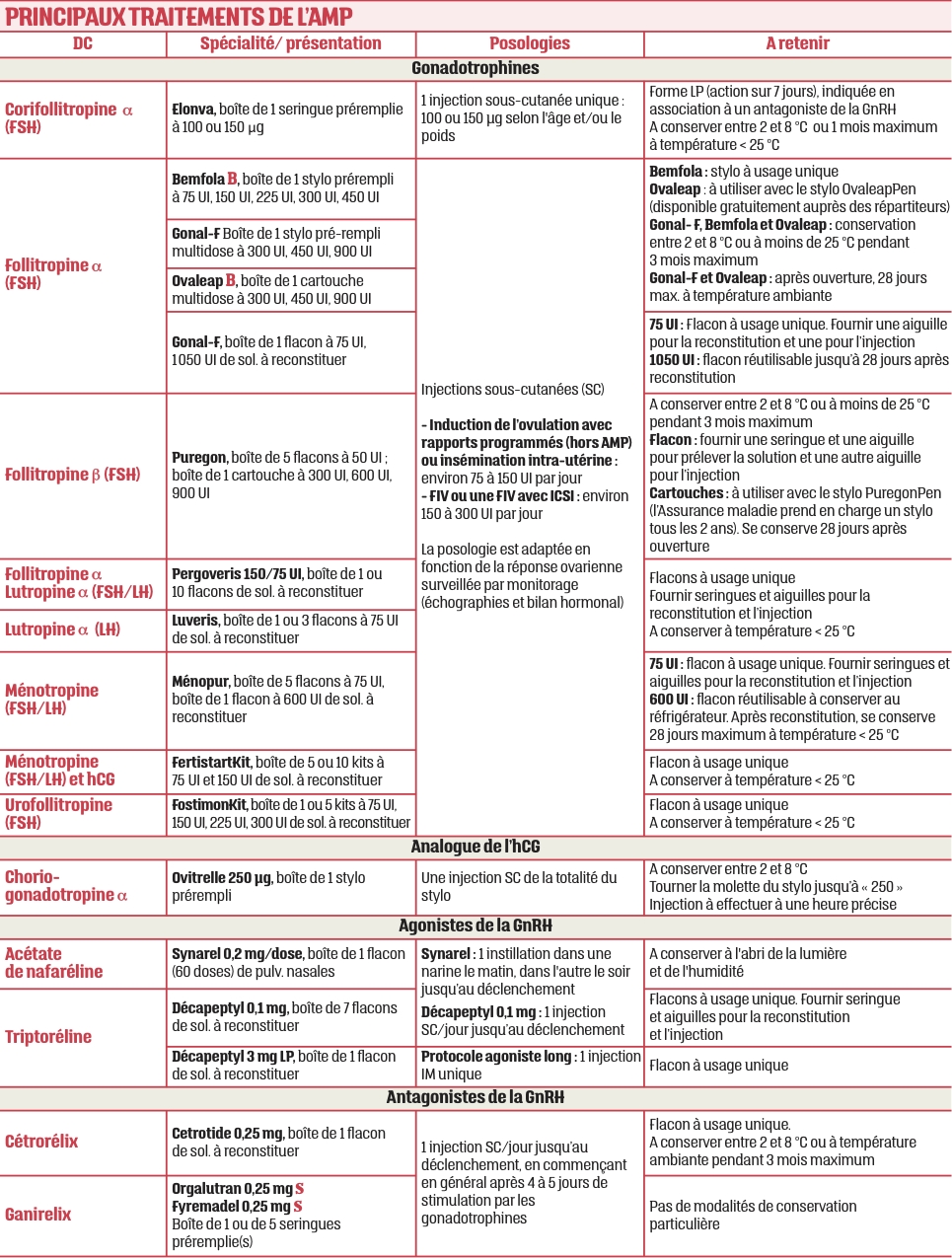
Sources : medicaments.gouv.fr. S : substituable. B : biosimilaire. Matériel complémentaire à fournir selon le cas : aiguille pour reconstitution : gauge 18 (rose), voire gauge 21 (verte) pour injection IM ; aiguille pour injection SC : gauge 25 (orange), 26 (marron) et 30 (jaune) ; seringue montée 1 ml (tuberculine) : gauge 26 (SC) ; seringue montée 2 ml : gauge 25 (SC), gauge 21 (IM ou reconstitution) ; seringue sans aiguille : 2 ml ou 1 ml.
Pourrez-vous respecter la minute de silence en mémoire de votre consœur de Guyane le samedi 20 avril ?
1Healthformation propose un catalogue de formations en e-learning sur une quinzaine de thématiques liées à la pratique officinale. Certains modules permettent de valider l'obligation de DPC.
Vous avez des questions ?
Des experts vous répondent !













